近日,广东医科大学附属东莞第一医院/第二临床医学院教授、东莞呼吸医学研究所所长赖天文团队在国际顶级学术期刊Nature子刊Nature Communications发表题为“Epithelial SIRT6 governs IL-17A pathogenicity and drives allergic airway inflammation and remodeling”(气道上皮SIRT6调控IL-17A致病性导致哮喘气道炎症及重构)的重要研究成果。这是我校师生首次以广东医科大学为独立完成单位在Nature 子刊发表重要成果。

Nature Communications《自然通讯》是国际顶级学术期刊Nature发行的子刊,是全球82本国际公认的、能够衡量机构、国家和地区在自然科学领域的高质量研究产出的“自然指数”(Nature Index)顶级期刊之一。该成果发表标志着团队的原始创新能力和科研能力迈上了全新的台阶,进入了更高的维度。

赖天文教授(右一)与课题组成员
支气管哮喘(简称哮喘)是严重危害人类健康的慢性气道炎症性疾病。我国最新流行病学调查表明:20岁及以上的哮喘患病率为4.2%。气道重塑是重症哮喘的重要病理特征,临床治疗棘手,但其发病机制仍未阐明。因此,针对哮喘发病机制、新的生物标志物及潜在干预靶点的研究亟待突破。赖天文教授团队研究成果首次揭示了SIRT6调控IL-17A致病性在哮喘气道炎症反应及气道重构中的作用机制,提示靶向SIRT6是哮喘的潜在治疗靶点。
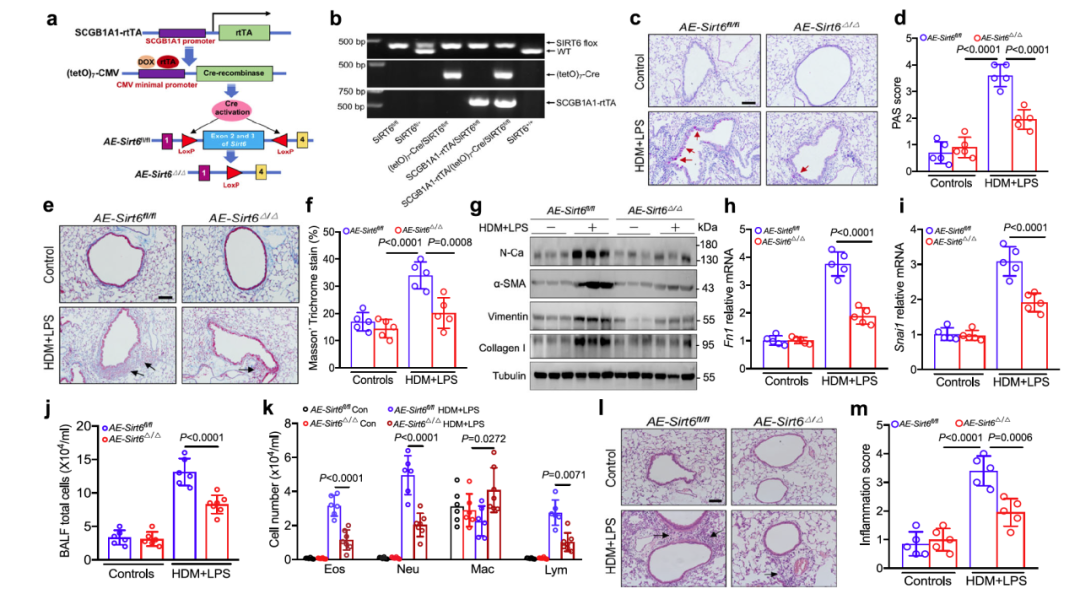
近年来,表观修饰介导的过敏原,微生物及空气污染物等环境暴露诱发哮喘的发病机制备受关注。表观修饰主要包括乙酰化、甲基化、磷酸化和泛素化等,其中组蛋白乙酰化修饰尤为重要。SIRT6 作为sirtuin去乙酰酶家族成员,在调节细胞增殖、应激反应、基因组稳定性、能量平衡和衰老方面起着主导作用。运用临床样本、转基因动物模型、组学与生物信息学等多种方法,发现SIRT6表达与哮喘患者气道重构和疾病严重程度呈正相关。气道上皮来源的SIRT6作为表观遗传调节因子,通过促进IL-17A介导的炎症趋化因子和间充质重编程,缓解哮喘气道炎症反应及气道重构。气道上皮细胞特异性敲除SIRT6或SIRT6抑制剂(OSS_128167)缓解哮喘小鼠气道炎症和气道重构。
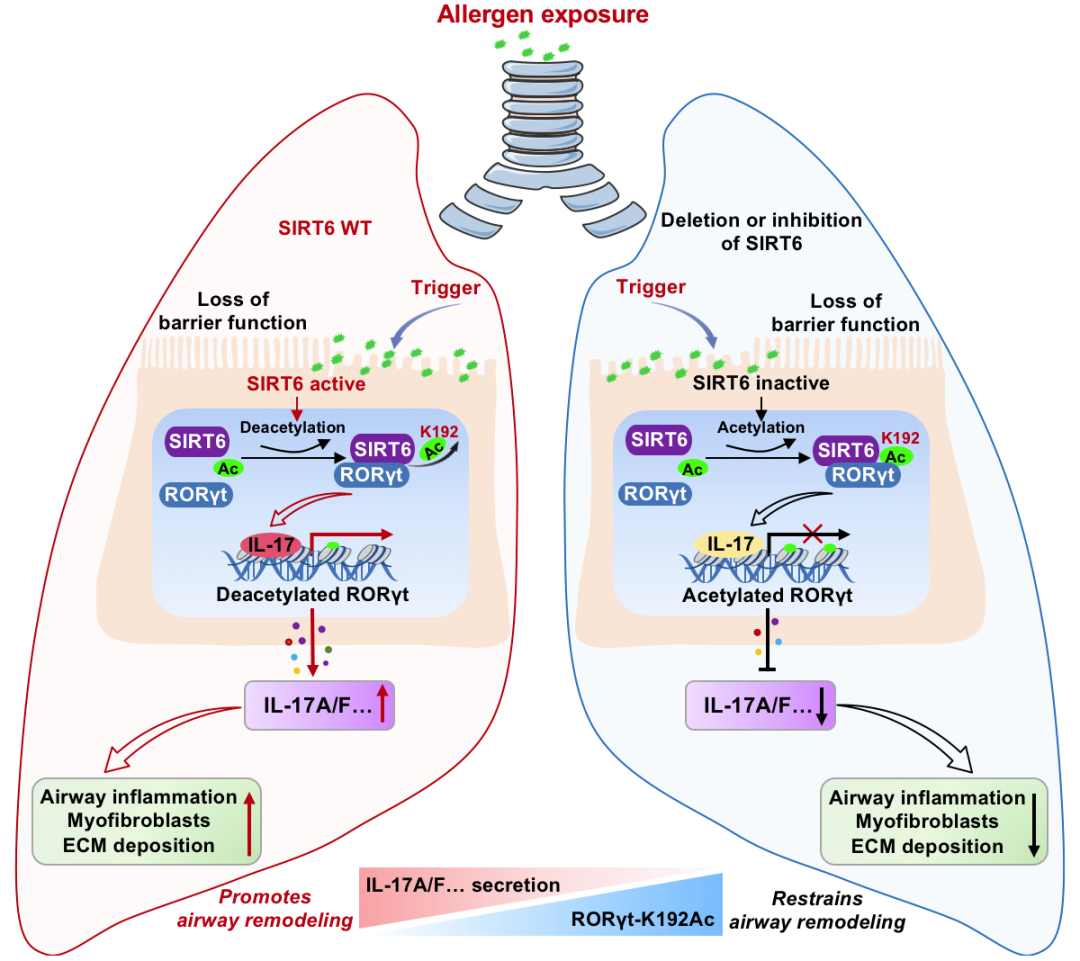
从机制上讲,SIRT6直接与RORγt相互作用,并通过PPXY基序在赖氨酸192处介导RORγt脱乙酰化,促进IL-17A基因启动子募集并增强其转录,导致哮喘气道炎症及气道重构发生。
广东医科大学近年来引进一批国家级人才,牵头组建了“生物医药与大健康湾区创新生态联盟”,创建东莞创新研究院成为集聚资源服务创新的重要平台、人才交流合作的创新俱乐部。创建了“广东医科大学-东莞理工学院松山湖医工融合创新中心”“广东医科大学-东莞理工学院医工联合创新学院”,并“上线”了广东首批3个联合学士学位培养项目。携手华为技术有限公司及其生态企业,共建健康医疗大数据工程中心。联动松山湖材料实验室,促进材料与生命科学跨界融合。启用广东医科大学-东莞兰卫医学检验实验室斑马鱼模式动物研究与创新应用实验室。获2项国家自然科学基金区域创新发展联合基金重点支持项目。
自2020年12月东莞市人民政府和广东医科大学签约开展校地共建以来,广东医科大学附属东莞第一医院在学科建设、队伍建设、平台建设等方面取得显著成效。校地共建前全院仅有2篇SCI论文,校地共建以来新发表SCI论文220篇。申请专利31项,获授权专利17项;出版译著、教材等著作16部。主持国自然基金5项(含东莞医疗机构首个区域联合基金重点支持项目1项),每年人均科研经费显著增长。(信源/第二临床医学院/附属东莞第一医院 编辑/陈瑶瑶 复核/周圆 审发/ 冯锦山)
